Tratamentul laparoscopic al chisturilor ovariene
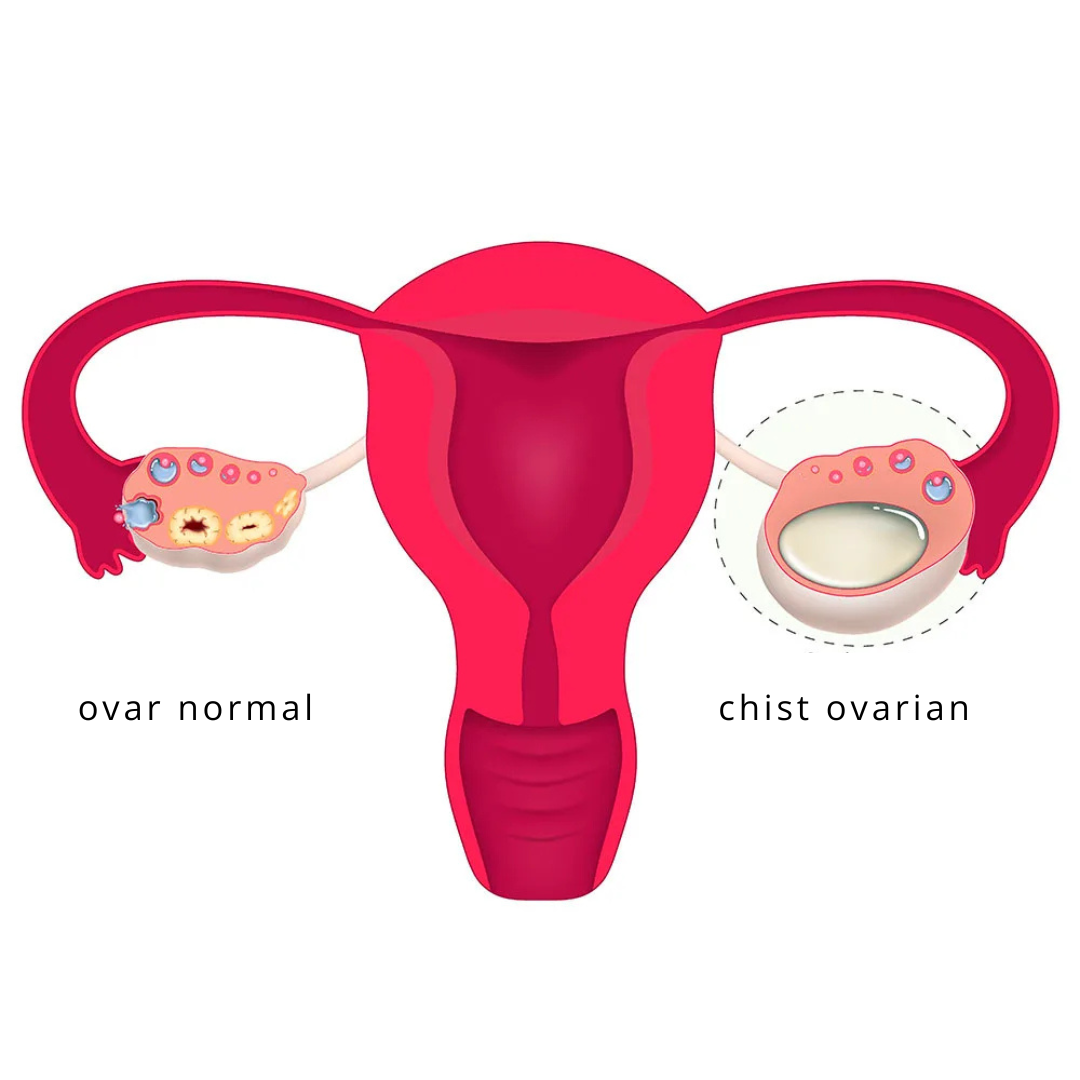
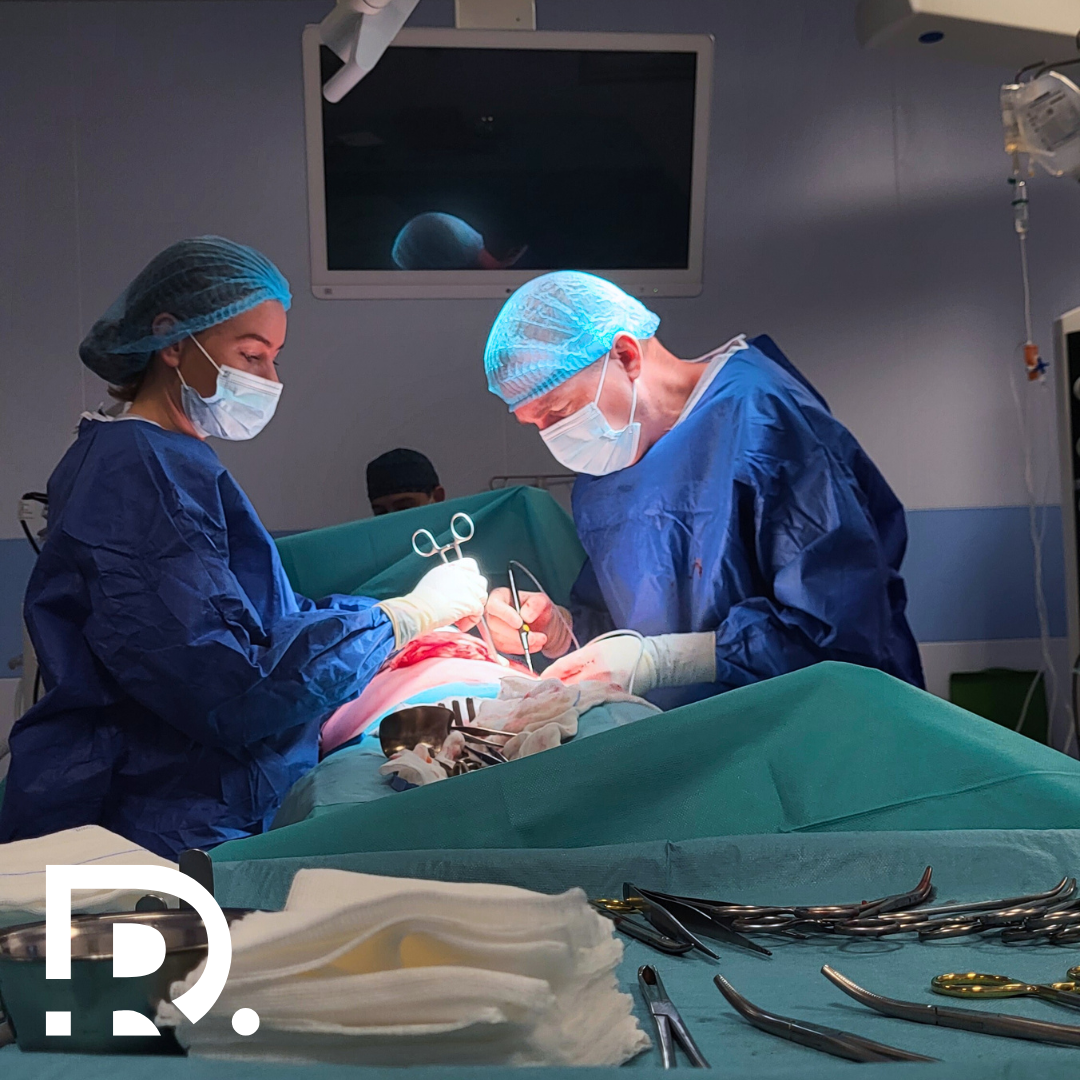
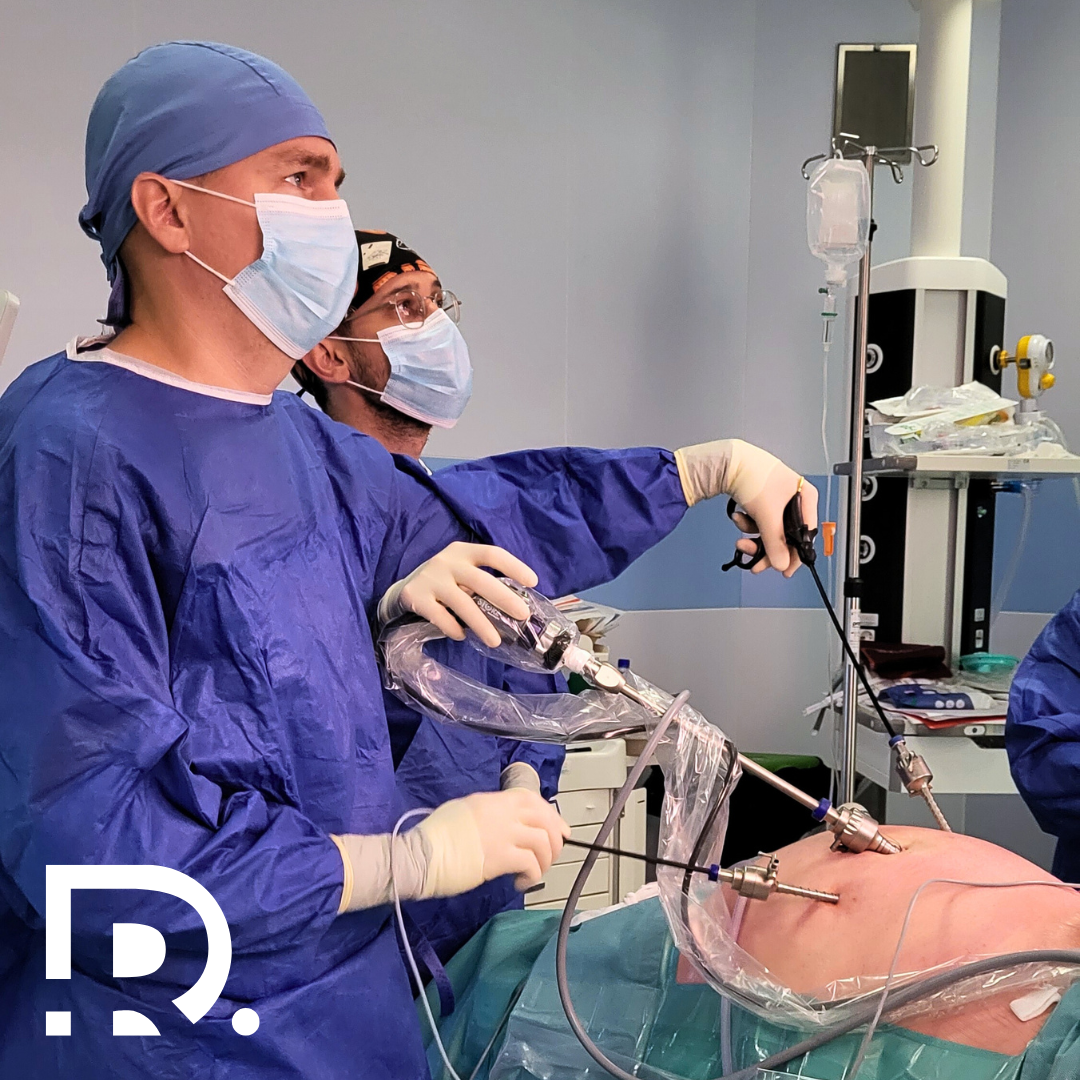
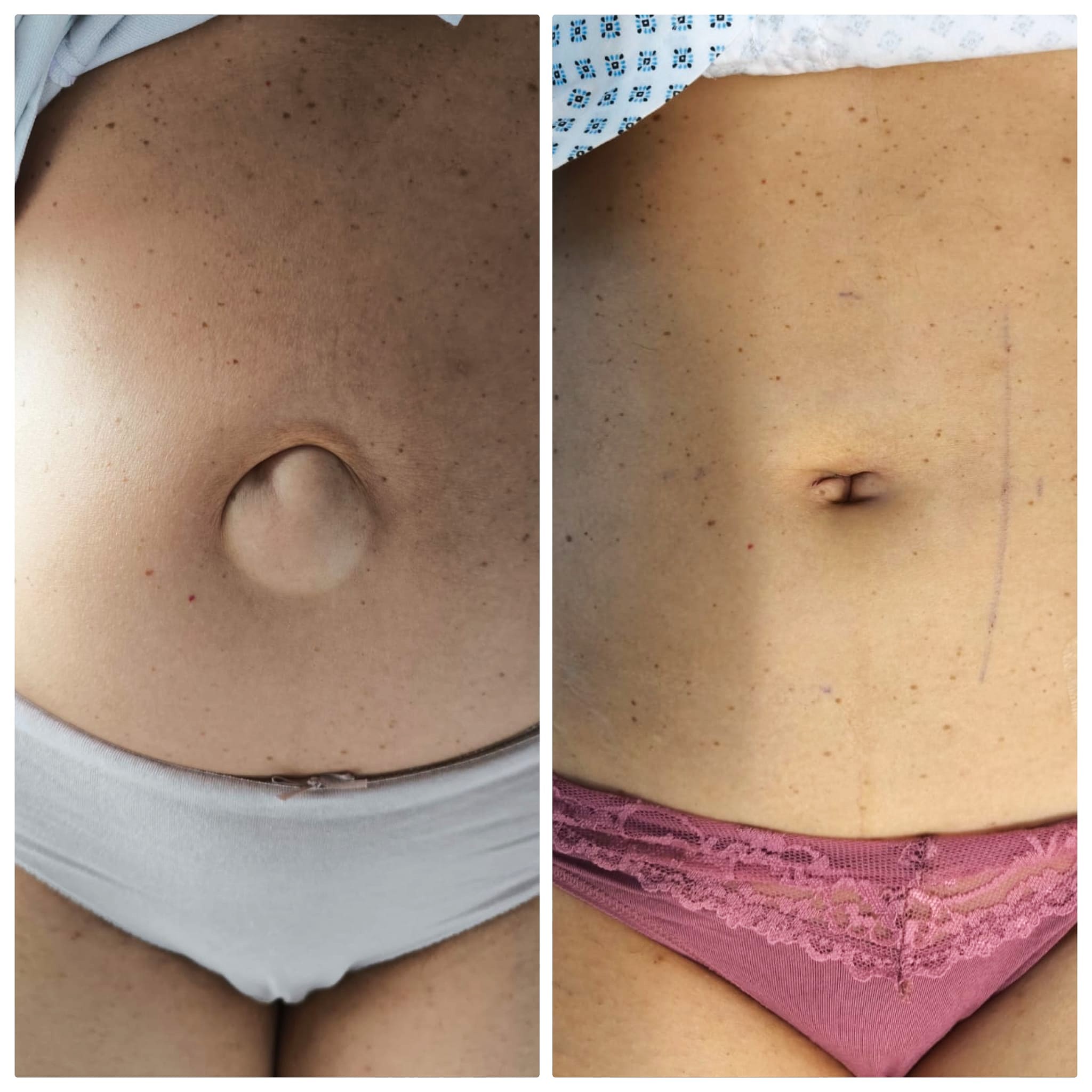
Chisturile ovariene sunt o afecțiune ginecologică frecventă care poate afecta femeile de toate vârstele. Deși majoritatea chisturilor sunt benigne și se rezolvă de la sine, unele pot provoca complicații, cum ar fi durere, balonare, menstruații neregulate sau chiar rupere, necesitând intervenție medicală. Odată cu progresele în tehnologia medicală, chirurgia laparoscopică a devenit metoda preferată pentru tratarea chisturilor ovariene, oferind o alternativă minim-invazivă, sigură și eficientă la intervenția chirurgicală clasică. În acest ghid complet, îți voi prezenta tot ce trebuie să știi despre tratamentul laparoscopic al chisturilor ovariene, inclusiv beneficiile, indicațiile, procedura chirurgicală, recuperarea, riscurile și îngrijirea postoperatorie. Dacă tu sau o persoană dragă ați fost diagnosticate cu un chist ovarian și iei în considerare intervenția chirurgicală, acest articol vă va oferi informații valoroase pentru a lua o decizie informată. Înțelegerea chisturilor ovariene: cauze și tipuri Chisturile ovariene sunt saci plini cu lichid care se dezvoltă pe sau în interiorul ovarelor. Acestea pot varia ca dimensiune și tip, iar unele necesită îndepărtare chirurgicală atunci când devin simptomatice sau prezintă riscuri pentru sănătate. Tipuri comune de chisturi ovariene 1. Chisturi funcționale: acestea sunt cele mai frecvente și apar ca parte a ciclului menstrual. Ele includ: 2. Chisturi dermoide (teratoame): conțin diferite tipuri de țesut, cum ar fi păr, piele și dinți. Acestea sunt de obicei benigne, dar pot crește în dimensiuni și necesita îndepărtare chirurgicală. 3. Endometrioame: cunoscut și sub denumirea de „chisturi de ciocolată”, acest tip de chist este asociat cu endometrioza și conține sânge vechi, de culoare închisă. 4. Cistadenom: tumori benigne care se dezvoltă pe suprafața ovarului și pot ajunge la dimensiuni considerabile. 5. Ovare polichistice: o afecțiune caracterizată prin formarea mai multor chisturi mici, cauzată de dezechilibre hormonale, frecvent întâlnită în Sindromul Ovarelor Polichistice (SOP). Când este necesară chirurgia laparoscopică? Majoritatea chisturilor ovariene dispar de la sine în câteva cicluri menstruale. Totuși, intervenția chirurgicală laparoscopică poate fi necesară în următoarele situații: Chirurgia laparoscopică pentru chisturile ovariene Laparoscopia, cunoscută și sub numele de „chirurgie minim-invazivă”, presupune realizarea unor incizii mici în abdomen pentru îndepărtarea chistului, păstrând ovarele intacte. Pregătirea preoperatorie Înainte de intervenția chirurgicală laparoscopică, pacienta trebuie să efectueze o serie de investigații, inclusiv: Etapele intervenției chirurgicale 1. Anestezie: procedura se efectuează sub anestezie generală, asigurându-se că pacienta este complet adormită și nu simte durere. 2. Incizii: chirurgul realizează 2-4 incizii mici (de obicei mai mici de 1 cm) în partea inferioară a abdomenului. 3. Introducerea laparoscopului: un tub subțire și flexibil cu o cameră video (laparoscop) este introdus printr-o incizie, permițând vizualizarea ovarelor pe un monitor. 4. Insuflarea gazului: abdomenul este umplut cu dioxid de carbon pentru a crea spațiu necesar manevrelor chirurgicale. 5. Îndepărtarea chistului: cu ajutorul unor instrumente speciale, chirurgul îndepărtează chistul cu grijă, păstrând țesutul ovarian sănătos. 6. Închiderea inciziilor: după verificarea eventualelor sângerări sau complicații, instrumentele sunt retrase, gazul este eliminat, iar inciziile sunt închise cu fire resorbabile. Beneficiile chirurgiei laparoscopice pentru chisturile ovariene Chirurgia laparoscopică a revoluționat gestionarea chisturilor ovariene datorită numeroaselor sale avantaje față de chirurgia deschisă tradițională. Această tehnică minim-invazivă nu doar că oferă o soluție eficientă pentru îndepărtarea chisturilor problematice, dar îmbunătățește și rezultatele pentru pacientă, reducând durerea, timpul de recuperare și riscul de complicații. Femeile care aleg îndepărtarea laparoscopică a chisturilor se bucură de o revenire mai rapidă la activitățile zilnice, un rezultat estetic îmbunătățit și un risc redus de complicații chirurgicale pe termen lung. Mai jos sunt prezentate principalele beneficii ale chirurgiei laparoscopice comparativ cu procedurile clasice deschise: 1. Abordare minim-invazivă În comparație cu chirurgia deschisă (laparotomia), laparoscopia necesită doar incizii mici—de obicei mai mici de un centimetru—prin care sunt introduse o cameră de dimensiuni reduse și instrumente chirurgicale specializate. Această tehnică reduce semnificativ trauma țesuturilor din jur, deoarece chirurgul poate îndepărta chistul cu grijă, păstrând în același timp țesutul ovarian sănătos. Deoarece inciziile sunt mult mai mici decât cele utilizate în chirurgia deschisă, pacienta se confruntă cu mai puține cicatrici interne, un risc redus de infecție a plăgii și o șansă mai mică de formare a aderențelor, care uneori pot duce la probleme de fertilitate sau dureri pelviene cronice. 2. Recuperare mai rapidă Unul dintre cele mai importante avantaje ale chirurgiei laparoscopice este timpul mai scurt de recuperare. Deoarece inciziile sunt mici și perturbarea organelor abdominale este minimă, pacientele se recuperează mult mai rapid decât după o intervenție deschisă. Cele mai multe femei pot relua activitățile ușoare zilnice în câteva zile și se pot întoarce la muncă sau la rutina obișnuită în 1-2 săptămâni. În schimb, chirurgia deschisă necesită o spitalizare de câteva zile, urmată de o perioadă de recuperare de 4-6 săptămâni. Această recuperare rapidă permite pacientelor să-și recapete mai repede calitatea vieții, fără a suferi întreruperi semnificative în activitățile personale sau profesionale. 3. Durere redusă Deoarece chirurgia laparoscopică este mai puțin invazivă, aceasta generează mult mai puțină durere postoperatorie comparativ cu chirurgia deschisă. Inciziile mai mici provoacă mai puține leziuni ale țesuturilor, ceea ce înseamnă că pacientele au o nevoie mai redusă de analgezice puternice, cum ar fi opioidele. Multe femei reușesc să gestioneze disconfortul postoperator cu medicamente fără prescripție medicală, precum ibuprofenul sau paracetamolul. Durerea redusă contribuie, de asemenea, la o revenire mai rapidă la activitățile zilnice, deoarece pacientele nu sunt afectate de un disconfort sever sau de o dependență prelungită de medicamente. 4. Risc mai mic de complicații Chirurgia laparoscopică este asociată cu un risc mai mic de complicații, inclusiv infecții, sângerare excesivă și formarea de aderențe. Inciziile mici reduc numărul de puncte de intrare pentru bacterii, diminuând astfel probabilitatea infecțiilor postoperatorii. În plus, datorită preciziei cu care este realizată intervenția, există un risc mai scăzut de afectare accidentală a organelor din apropiere, cum ar fi vezica urinară, intestinul sau trompele uterine. O altă preocupare majoră legată de chirurgia deschisă este formarea aderențelor—benzi de țesut cicatricial care pot provoca dureri și infertilitate. Natura minim-invazivă a laparoscopiei ajută la reducerea formării aderențelor, contribuind la menținerea sănătății reproductive a femeilor mai tinere care doresc să aibă copii în viitor. 5. Rezultat estetic îmbunătățit Deoarece chirurgia laparoscopică necesită doar câteva incizii mici în locul unei … Read more