De ce apare apendicita?
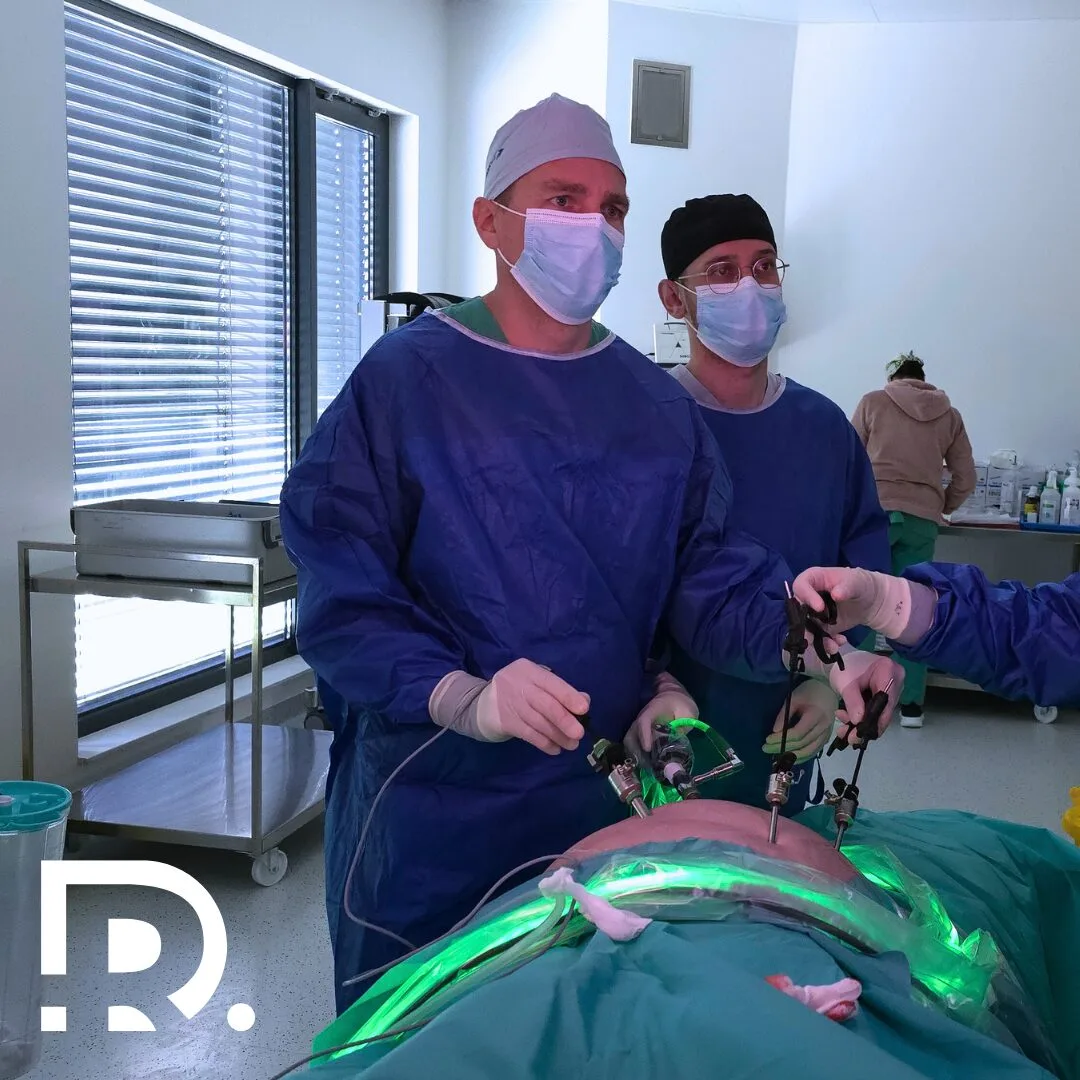
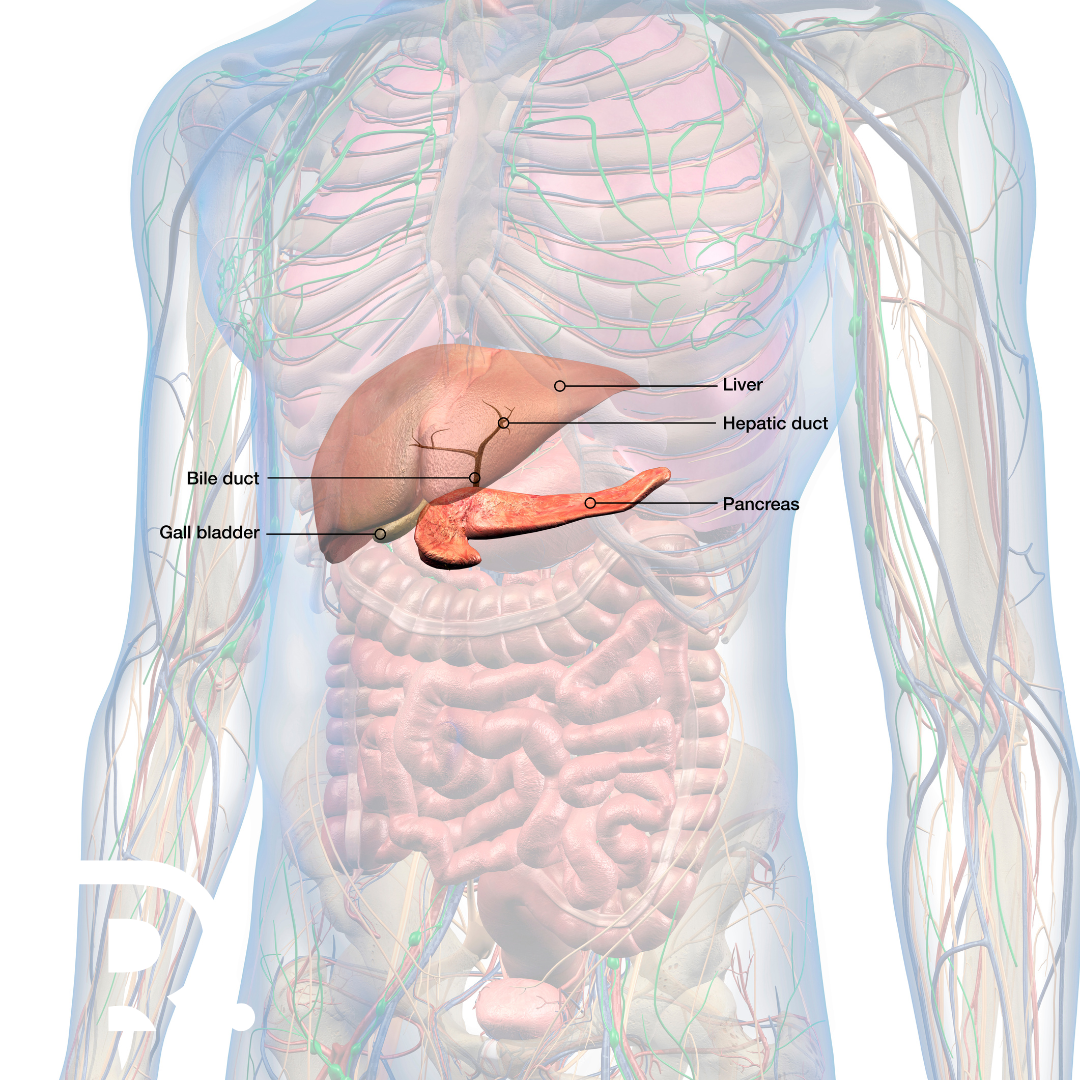
Apendicita este o urgență chirurgicală care afectează aproximativ 7% din populație în cursul vieții. Deși apendicele este un organ mic, situat în partea dreaptă jos a abdomenului, inflamația sa poate deveni rapid o problemă gravă, cu risc de complicații fatale. Ca medic primar chirurgie generală, specializat în chirurgia minim-invazivă (laparoscopică și robotică), întâlnesc frecvent pacienți care subestimează simptomele inițiale, ajungând la spital în stadiu avansat. Acest articol vă va dezvălui mecanismele din spatele apendicitei, semnele de avertizare și avantajele intervențiilor moderne. Dacă aveți dureri abdominale persistente, nu amânați consultul medical – o perforație a apendicelui poate duce la infecții generalizate în doar 48 de ore! Ce este apendicita și care este rolul apendicelui? Structura și localizarea apendicelui Apendicele este un organ tubular subțire, cu o lungime între 5 și 10 cm, situat în partea dreaptă a abdomenului. Este atașat de cecum – prima porțiune a colonului, la nivelul unde intestinul subțire se conectează cu cel gros. Poziția sa exactă poate varia: în 65% din cazuri, apendicele este retrocecal (se află în spatele cecului), dar poate fi și pelvian (coborât în regiunea pelvică) sau subhepatic (sub ficat). Această variabilitate anatomică explică de ce uneori simptomele apendicitei pot fi confundate cu alte afecțiuni abdominale. Funcția apendicelui: mai mult decât un organ vestigial Mult timp, apendicele a fost considerat un organ vestigial, fără funcție relevantă. Însă cercetările recente au demonstrat că are un rol important în sistemul imunitar și în menținerea sănătății intestinale. Apendicele adăpostește o rezervă de bacterii benefice (microbiota intestinală), care pot repopula colonul după episoade de diaree sau tratamente cu antibiotice. De asemenea, produce celule imune și imunoglobuline (anticorpi), care contribuie la apărarea organismului împotriva patogenilor. Aceste descoperiri au schimbat percepția asupra acestui organ, deși inflamația sa – apendicita – rămâne o urgență medicală frecventă și imprevizibilă. Cum se dezvoltă apendicita? Apendicita apare atunci când lumenul (spațiul interior) apendicelui se blochează. Obstrucția poate fi cauzată de fecalite (bucăți de materie fecală uscată), hiperplazia limfoidă (umflarea țesutului limfoid) sau corpuri străine (semințe, paraziți). Blocajul duce la acumularea de mucus și creșterea presiunii în interiorul apendicelui. Acest lucru compromite fluxul sanguin (ischemie), iar țesutul, lipsit de oxigen și nutrienți, începe să se necrozeze. Dacă obstrucția persistă, peretele apendicelui se perforează în aproximativ 48-72 de ore, iar bacteriile din interior (precum Escherichia coli) se răspândesc în cavitatea abdominală. Aceasta declanșează o infecție severă (peritonită) sau formarea de abcese, punând viața pacientului în pericol. Cauzele apendicitei: de la blocaje la infecții Apendicita apare în majoritatea situațiilor din cauza obstrucției lumenului apendicelui – canalul îngust prin care circulă mucusul și alte secreții. Această blocare poate fi declanșată de mai mulți factori, iar mecanismul exact variază în funcție de situație. Fecalitele sunt una dintre cele mai frecvente cauze. Acestea sunt aglomerări compacte de materii fecale, săruri minerale și fibre care se usucă și se întăresc în timp. Persoanele cu o dietă săracă în fibre sau cu hidratare insuficientă au un risc crescut, deoarece fibrele mențin materia fecală moale, iar lichidele facilitează eliminarea acesteia. Când fecalitele se acumulează în apendice, ele blochează fluxul natural, creând o presiune crescândă care duce la inflamație. Hiperplazia limfoidă este un alt mecanism important. Țesutul limfoid din peretele apendicelui se poate umfla excesiv ca răspuns la infecții virale sau bacteriene, precum gastroenterita. Această umflătură reduce diametrul lumenului, blocând trecerea secrețiilor. Deși hiperplazia este adesea temporară, în unele cazuri poate persista suficient de mult pentru a declanșa apendicita. Corpurile străine nu trebuie ignorate. Semințele neingestate, paraziții intestinali (cum ar fi viermii oxiuri) sau chiar calculi biliari migrați pot obstrucționa apendicele. Acestea acționează ca un dop fizic, perturbând funcția normală a organului. Odată ce obstrucția este stabilită, infecțiile bacteriene devin inevitabile. Blocajul favorizează proliferarea rapidă a bacteriilor precum Escherichia coli, Klebsiella pneumoniae și Pseudomonas aeruginosa. Aceste microbiote intestinale patogene invadează peretele apendicelui, provocând inflamație purulentă, necroză tisulară și, în final, perforație. Fără intervenție, bacteriile se răspândesc în cavitatea abdominală, ducând la peritonită sau sepsis. Factori de risc ascunși pot crește probabilitatea apariției apendicitei. De exemplu, vârsta joacă un rol crucial: 70% din cazuri apar la persoanele între 10 și 30 de ani, probabil datorită anatomiei apendicelui (lumen mai îngust) și expunerii frecvente la infecții gastrointestinale în această perioadă. Totuși, copiii sub 5 ani și adulții peste 50 de ani nu sunt excluși – la aceștia, diagnosticul este adesea întârziat din cauza simptomelor atipice. Predispoziția genetică este de asemenea semnificativă. S-a observat că persoanele cu antecedente familiale de apendicită au risc crescut, probabil datorită moștenirii unor trăsături anatomice (apendice mai lung sau tortuos) sau a unor particularități ale sistemului imun. Bolile inflamatorii intestinale cronice, precum colita ulcerativă sau boala Crohn, pot contribui indirect. Inflamația persistentă a colonului se extinde uneori și la apendice, slăbind peretele său și facilitând infecțiile. Nu subestimați o durere abdominală care persistă peste 6 ore! Apendicita poate evolua rapid spre complicații. Simptomele apendicitei: de la semne clasice la variante atipice Simptomele tipice ale apendicitei încep cu durere periombilicală (în jurul buricului), care migrează în cadran inferior drept al abdomenului în 12-24 de ore. Febra moderată (37.5-38.5°C) este însoțită de frisoane și transpirații. Aproape 90% dintre pacienți raportează pierderea apetitului și grețuri. Un semn clinic specific este semnul Blumberg – durerea care apare la eliberarea bruscă a presiunii în zona afectată. Cazurile atipice pot face diagnosticul mai dificil. La copii, durerea este adesea mai difuză, iar febra poate depăși 39°C. La femeile însărcinate, poziția apendicelui este modificată datorită uterului mărit, iar durerea poate fi confundată cu contracții. La persoanele în vârstă, semnele pot fi atenuate din cauza răspunsului imun slab. Durerea care se intensifică la mișcare, tuse sau respirație adâncă indică iritarea peritoneului – un motiv de intervenție imediată. Diagnosticul apendicitei: pași esențiali pentru evitarea erorilor Diagnosticul începe cu un examen clinic amănunțit. Medicul evaluează sensibilitatea localizată, prezența rigidității abdominale și semne specifice, precum semnul Rovsing (durere în partea dreaptă la palparea părții stângi). Investigațiile de laborator, precum hemograma, pot confirma inflamația prin creșterea leucocitelor (>10.000/mm³) și a neutrofilelor (>75%). Proteina C reactivă (PCR) este un alt marker important, cu valori … Read more